第六章 立体化学
一、异构体的分类
1. 同分异构的定义
分子式相同但原子排列(连接顺序或空间排布)不同的化合物,称为同分异构体。
2. 异构类型分类
| 异构层级 | 类型 | 定义 | 示例 |
|---|---|---|---|
| 一级异构 | 构造异构 | 原子/基团连接顺序不同,构造式不同 | 正丁烷与异丁烷 |
| 二级异构 | 立体异构(构型+构象) | 构造式相同,原子/基团空间排布不同 | —— |
| - 构型异构 | 空间排布需断裂化学键才能改变,不可通过σ键旋转互变 | 烯烃顺反异构、对映异构 | |
| - 构象异构 | 空间排布通过σ键旋转即可改变,为分子不同构象状态 | 乙烷交叉式与重叠式 | |
| 三级异构 | 构型异构细分 | - 对映异构体:互为镜像且不能重合的构型异构体 | -丁-2-醇与-丁-2-醇 |
| - 非对映异构体:非镜像关系的构型异构体 | 麻黄碱与-麻黄碱 |
二、手性和对称性
1. 手性与对映异构
- 手性分子:与自身镜像不能重合的分子,具有手性。
- 手性碳原子(C)*:连有四个不同原子或基团的饱和碳原子,是手性分子的常见来源(例:2-溴丁烷的C2,结构为)。
- 对映体:手性分子的两种构型异构体,互为镜像且不能重合,如左旋2-溴丁烷[(-)-2-溴丁烷]与右旋2-溴丁烷[(+)-2-溴丁烷]。
2. 对称因素(判断分子手性的核心)
分子若存在对称面或对称中心,则为非手性分子(无对映异构);反之则为手性分子。
- 对称面(σ):能将分子分为互为镜像两半的平面。
例:(E)-1,2-二氯乙烯(分子所在平面为对称面)、二氯甲烷(2个对称面:Cl-C-Cl平面与H-C-H平面)。 - 对称中心(i):分子中心一点,从任意原子向中心作线,延长等距离必遇相同原子。
例:(E)-1,2-二氯乙烯(C-C双键中心为对称中心)、1,3-二氯丙烷(分子中心为对称中心)。
三、手性分子的性质——光学活性
1. 旋光性
- 平面偏振光:单色光通过Nicol棱镜后,仅在单一平面振动的光。
- 旋光性物质:能使平面偏振光振动平面旋转的物质(手性分子纯品),分为:
- 右旋体:使偏振光顺时针旋转(迎着光线),标记为。
- 左旋体:使偏振光逆时针旋转,标记为。
- 外消旋体(±):等物质的量左旋体与右旋体的混合物,旋光性相互抵消,无光学活性,可通过特定方法拆分为单一对映体。
2. 比旋光度(手性分子的特征物理常数)
(1)定义
在特定温度()和光源波长(常用钠光D线,589nm,标记为)下,1mL含1g溶质的溶液在1dm长盛液管中产生的旋光度,是衡量旋光能力的指标。
(2)计算公式
- :比旋光度(单位:);
- :旋光仪测得的旋光度(单位:);
- :溶液质量浓度(单位:,纯液体用密度替代);
- :盛液管长度(单位:)。
(3)示例
- 葡萄糖水溶液:(水为溶剂);
- 薯皂苷元氯仿溶液():(为溶剂)。
四、含一个手性中心化合物的对映异构
1. 构型表示法
(1)透视式(楔形键式)
- 手性碳置于纸面,连有四个键:
- 细实线:键在纸面内;
- 楔形实线:键伸向纸面前方;
- 楔形虚线:键伸向纸面后方。
例:
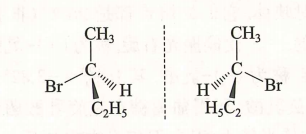
(2)Fischer投影式(平面表示立体)
- 规则:
- 手性碳为横竖线交点,竖线基团伸向纸面后方,横线基团伸向纸面前方;
- 主碳链置于竖线,命名时编号最小的碳原子(如羧基、醛基)放在上端。
例:
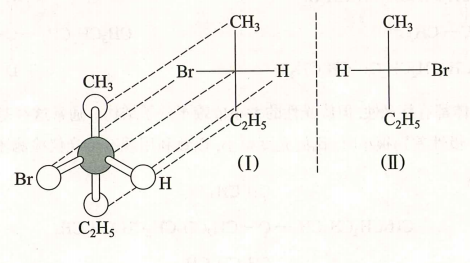
2. 构型标记法
(1)D,L-标记法(相对构型,多用于糖类、氨基酸)
- 标准:以甘油醛为基准,Fischer投影式中羟基在右侧为D型,左侧为L型。
- 关联:通过不涉及手性碳的化学反应,可将目标化合物与D/L-甘油醛关联,确定其D/L构型(例:D-(+)-甘油醛可转化为D-乳酸)。
- 局限性:部分化合物难以与甘油醛关联,易产生歧义。
(2)R,S-标记法(绝对构型,通用)
步骤:
- 按次序规则排序:将手性碳连的四个基团(a,b,c,d)按原子序数从大到小排序(a>b>c>d,d为最不优先基团);
- 定向:将最不优先基团d置于距观察者最远的位置;
- 判断构型:观察a→b→c的排列方向,顺时针为R型(拉丁文rectus,“右”),逆时针为S型(拉丁文sinister,“左”)。
示例:丁-2-醇():
- 基团排序:(a)>(b)>(c)>(d);
- d(H)远离观察者,a→b→c顺时针为R型,逆时针为S型;
- 注意:R,S构型与旋光方向(+/-)无必然联系(例:-丁-2-醇可能为左旋或右旋)。
五、含两个手性中心化合物的构型异构
1. 含两个不同手性中心的化合物
- 异构体数目:最多4种(),分为2对对映体,不同对映体间为非对映体。
- 对映体:互为镜像且不能重合(例:氯代苹果酸的(I)与(II));
- 非对映体:非镜像关系的构型异构体,物理性质(熔点、溶解度、旋光度)不同(例:氯代苹果酸的(I)与(III))。
示例:麻黄碱(2-甲氨基-1-苯基丙-1-醇):
- 2个不同手性碳,4种异构体:
- (1)与(II):对映体(麻黄碱),熔点34°C,盐酸盐;
- (III)与(IV):对映体(ψ-麻黄碱),熔点118°C,盐酸盐;
- (I)/(II)与(III)/(IV):非对映体。
2. 含两个相同手性中心的化合物
- 异构体数目减少:因分子内可能存在对称面,产生内消旋体,实际异构体数目少于4种。
示例:酒石酸(2,3-二羟基丁二酸,):
-
2个相同手性碳,仅3种异构体:
- 右旋体:(R,R)构型,熔点170°C,溶解度139g/(100g水),;
- 左旋体:(S,S)构型,与右旋体物理性质相同,旋光方向相反;
- 内消旋体(meso):(R,S)构型,分子内存在对称面,旋光性相互抵消,无光学活性,熔点140°C,溶解度125g/(100g水)。
-
内消旋体与外消旋体的区别:
特征 内消旋体(meso) 外消旋体(±) 本质 单一分子(分子内抵消旋光) 左旋体与右旋体的混合物 光学活性 无 无 可拆分性 不可拆分 可通过手性方法拆分 熔点 低于对映体(例:140°C) 高于对映体(例:204°C)
六、脂环化合物的立体异构
1. 脂环化合物的顺反异构
- 成因:环的刚性限制环内C-C σ键旋转,环上取代基位置不同产生顺反异构。
- 定义:取代基在环同侧为顺式(cis-),异侧为反式(trans-)。
示例:1,4-二甲基环己烷:
- 顺式:一个甲基在e键,一个在a键(构象:),稳定性较低;
- 反式:两个甲基均在e键(优势构象:),e键排斥小,稳定性更高。
2. 脂环化合物的对映异构
- 判断依据:分子无对称面/对称中心则为手性分子,存在对映体。
示例:1,2-二甲基环己烷:
- 顺式:分子存在对称面,为内消旋体(非手性),无光学活性;
- 反式:分子无对称因素,存在一对对映体((1R,2R)与(1S,2S)),均有光学活性,等物质的量混合为外消旋体。
示例:环丙烷-1,2-二甲酸:
- 顺式:内消旋体,熔点139°C,无光学活性;
- 反式:对映体,熔点175°C,可拆分,比旋光度。
七、不含手性中心化合物的对映异构(轴手性)
部分分子无手性碳,但存在手性轴(分子绕轴旋转180°后与原分子不重合),产生对映异构。
1. 丙二烯型化合物
- 结构特征:累积双键(),两端碳原子(C1、C3)各连两个不同基团,C1、C2、C3的p轨道垂直,C1/C3所在平面相互垂直。
- 构型标记(Rₐ/Sₐ):
- 沿手性轴一端观察,将基团按次序规则分为“近处优先”(1>2)和“远处优先”(3>4);
- 将最不优先基团(4)远离观察者,观察1→2→3的方向,顺时针为,逆时针为。
例:戊-2,3-二烯(),存在和对映体。
2. 联苯型化合物
- 结构特征:两个苯环通过C-C σ键连接,邻位有大体积取代基(如Br、Cl),阻碍σ键旋转,两苯环不共平面,且每个苯环不对称取代。
- 构型标记(Rₐ/Sₐ):与丙二烯型一致,若邻位取代基体积小(如F),则σ键可自由旋转,无对映异构。
例:2,2’-二溴-6,6’-二氯联苯,存在和对映体;2-溴-2’,6,6’-三氯联苯(一苯环对称取代),有对称面,无对映异构。
八、手性中心的产生
1. 第一个手性中心的产生(从非手性底物)
- 过程:非手性分子中,前手性碳(连两个相同基团的饱和碳,如)的一个相同基团被取代,生成手性碳。
- 结果:生成等量对映体,即外消旋体(非手性环境中,取代概率均等)。
例:正丁烷()光氯化,C2上一个H被Cl取代,得外消旋2-氯丁烷()。
2. 第二个手性中心的产生(从手性底物)
- 过程:已有手性中心的分子中,另一碳原子被取代,生成第二个手性碳。
- 结果:生成非对映体,且物质的量不等(手性环境影响试剂进攻方向)。
例:-2-氯丁烷()氯化,C3上H被Cl取代:- 产物:(2R,3R)-2,3-二氯丁烷(旋光体)与(2R,3S)-2,3-二氯丁烷(内消旋体);
- 比例:29:71(非对映体过量)。
九、不对称合成
1. 基本概念
- 不对称合成:在手性环境(手性底物、手性试剂、手性催化剂)中合成手性分子,使对映体/非对映体产量不等,直接获得具有光学活性的产物。
- 外消旋体拆分:将外消旋体通过手性试剂转化为非对映体,经物理方法(结晶、色谱)分离后,解离手性试剂得单一对映体。
2. 对映体过量(ee)与非对映体过量(de)
(1)对映体过量(ee,衡量对映选择性)
- 、:R型、S型对映体的浓度;
- 示例:某丁-2-醇试样,纯(S)-丁-2-醇,则(含75% S型、25% R型)。
(2)非对映体过量(de,衡量非对映选择性)
- 示例:-2-氯丁烷氯化得(2R,3R)与(2R,3S),。
3. 常用不对称合成方法
- 手性催化剂:如Sharpless不对称环氧化(Ti(OPr-i)₄为催化剂,手性配体调控)、Rh手性配合物催化氢化;
- 生物催化:酶(如脂肪酶)催化,立体选择性高;
- 手性试剂:如(-)-3-异松藏基硼烷(硼氢化试剂),生成光学活性醇。
重要背景:2001年诺贝尔化学奖授予Knowles(不对称催化氢化)、Sharpless(不对称环氧化)、野依良治(不对称氢化),表彰其在不对称合成领域的贡献。
十、对映异构在研究反应机理中的应用
1. 验证反应立体化学(以烯烃加溴为例)
- (Z)-丁-2-烯加溴:生成(2S,3S)-2,3-二溴丁烷与(2R,3R)-2,3-二溴丁烷(一对对映体,可拆分);
- (E)-丁-2-烯加溴:生成(2R,3S)-2,3-二溴丁烷(内消旋体,不可拆分);
- 结论:烯烃与溴加成为反式加成(仅反式加成可解释上述产物构型)。
2. 立体专一性与立体选择性
| 类型 | 定义 | 示例 |
|---|---|---|
| 立体专一性反应 | 构型异构体反应物,在相同条件下生成不同构型异构体产物 | (Z)/(E)-丁-2-烯加溴 |
| 立体选择性反应 | 反应物无特定构型要求,反应主要生成一种/少数几种构型异构体产物 | 癸-5-炔液氨中Na还原得80%反式烯烃 |
| 关系 | 立体专一性反应一定是立体选择性反应,反之则不一定 | —— |
