第七章 卤代烃
一、卤代烃的分类和命名
1. 卤代烃的定义
烃分子中一个或多个氢原子被卤原子(F、Cl、Br、I)取代的化合物,官能团为卤原子,通式为 R−X(或芳基卤代烃 Ar−X)。氟代烃因制法、性质特殊,单独讨论。
2. 分类
(1)按烃基结构分类
| 类别 |
细分类型 |
定义 |
示例 |
| 饱和卤代烃 |
- |
饱和烃(烷烃/环烷烃)的氢被卤原子取代 |
氯乙烷(CHX3CHX2Cl)、溴环己烷(CX6HX11Br) |
| 不饱和卤代烃 |
乙烯型 |
卤原子直接连双键碳(sp2 杂化) |
氯乙烯(CHX2=CHCl) |
|
烯丙型 |
卤原子与双键隔 1 个饱和碳 |
烯丙基氯(CHX2=CHCHX2Cl) |
|
隔离型 |
卤原子与双键隔 2 个及以上饱和碳 |
4-氯丁-1-烯(CHX2=CHCHX2CHX2Cl) |
| 卤代芳烃 |
苯基型 |
卤原子直接连苯环碳(sp2 杂化) |
氯苯(CX6HX5Cl) |
|
苄基型 |
卤原子与苯环隔 1 个饱和碳 |
苄基溴(CX6HX5CHX2Br) |
|
隔离型 |
卤原子与苯环隔 2 个及以上饱和碳 |
3-苯基-1-氯丙烷(CX6HX5CHX2CHX2CHX2Cl) |
(2)按卤原子连接碳原子类型分类
- 伯卤代烃(1°):卤原子连伯碳(R−CHX2−X),如 1-氯丙烷(CHX3CHX2CHX2Cl);
- 仲卤代烃(2°):卤原子连仲碳(R−CH(X)−RX′),如 2-溴丁烷(CHX3CHBrCHX2CHX3);
- 叔卤代烃(3°):卤原子连叔碳(RX3C−X),如叔丁基氯((CHX3)X3CCl)。
3. 命名
(1)普通命名法(习惯命名法)
- 规则:“烃基 + 卤原子”,直接命名简单卤代烃。
- 示例:异丙基溴((CHX3)X2CHBr)、叔丁基氯((CHX3)X3CCl)、烯丙基溴(CHX2=CHCHX2Br)。
- 俗名:多卤代烷常用俗名,如 CHClX3(氯仿)、CHBrX3(溴仿)、CHIX3(碘仿)、CClX4(四氯化碳)。
(2)系统命名法
- 规则:以烃为母体,卤原子为取代基,编号遵循“位次最小”原则。
- 卤代烷:选含卤原子的最长碳链,如 CHX3CH(Cl)CHX2CHX3(2-氯丁烷);
- 卤代环烷:环为母体,卤原子、烷基为取代基,如 1-甲基-4-溴环己烷(结构用图表示更合适);
- 卤代烯烃:选含双键和卤原子的最长碳链,双键编号优先,如 CHX3CH(Br)CH=CHX2(3-溴丁-1-烯);
- 卤代芳烃:苯环为母体,卤原子、烷基为取代基(具体结构建议配图),如 4-溴-2-氯乙基苯(仅示规则)。
二、卤代烃的制法
1. 烃的卤化
- 烷烃自由基卤化:烷烃在光照/高温下与卤素反应,生成混合卤代烷,如:
CHX3CHX2CHX3+ClX2hvCHX3CHX2CHX2Cl+(CHX3)X2CHCl
- 芳烃亲电卤化:苯环在 FeXX3 催化下与卤素反应,生成卤代芳烃,如:
CX6HX6+BrX2FeBrX3CX6HX5Br+HBr(126–142∘C)
- 烯烃烯丙位卤化(烯丙型卤代烃):高温条件下发生烯丙位取代,如:
CHX3CH=CHX2+ClX2500X∘CClCHX2CH=CHX2+HCl
2. 不饱和烃加成
- 亲电加成:烯烃/炔烃与 HX、XX2 加成;HX 加成通常符合马氏规则,如:
CHX3CH=CHX2+HBrHX2SOX4(CHX3)X2CHBr
CHX2=CHX2+BrX2CClX4BrCHX2CHX2Br
- 自由基加成:烯烃与 HBr 在过氧化物存在下反马氏加成,如:
CHX3CH=CHX2+HBrROORCHX3CHX2CHX2Br
3. 由醇制备(最常用)
- 与氢卤酸(HX)反应:可逆反应,叔醇反应最快,如:
(CHX3)X3COH+HCl(CHX3)X3CCl+HX2O
CX6HX11OH+HBrrefluxCX6HX11Br+HX2O
- 与卤化磷(PClX3、PBrX3)反应:避免重排,如:
3ROH+PBrX33RBr+HX3POX3
- 与氯化亚砜(SOClX2)反应:副产物为气体,产物纯度高,如:
ROH+SOClX2RCl+SOX2↑+HCl↑
4. 卤原子交换反应
5. 多卤代烃脱卤化氢
- 部分脱 HX 生成不饱和卤代烃(示意):
BrCHX2CHBrCHX3NaOH, HX2O, ΔCHX2=CBrCHX3+HBr
- 邻二卤代烷脱 2 分子 HX 生成炔烃(示意):
RCHX2CHXX2NaNHX2, NHX3(l)RC≡CH+2NaX+2NHX3
6. 其他方法
三、卤代烃的物理性质
1. 状态与颜色
- 氟代烃除外,CHX3Cl、CHX3Br、CHX2=CHCl 为气体;其余多为无色液体或固体。
- 碘代烷/溴代烷长期放置易分解,产生游离碘/溴而显色(碘代烷呈棕色)。
2. 溶解性与气味
- 不溶于水,溶于乙醇、乙醚、苯、四氯化碳等有机溶剂;部分卤代烃(CHX2ClX2、CHClX3)本身是优良溶剂。
- 多数有不愉快气味;部分卤代烃有毒(如氯乙烯);苄基型/烯丙型卤代烃常有催泪性。
3. 沸点与相对密度(核心规律)
| 性质 |
规律 |
| 沸点 |
碳数增加而升高;同碳数:RI>RBr>RCl>RF;异构体:支链越多沸点越低 |
| 相对密度 |
一氯代烷(<1),一溴代烷/一碘代烷(>1);卤代芳烃(>1);同系列中随碳数增加而下降 |
4. 偶极矩
- C−X 键有极性,偶极矩:CHX3Cl(4.84×10−30 C⋅m)> CHX3Br > CHX3I;
- 乙烯型卤代烃(如 CHX2=CHCl)因 p–π 共轭,偶极矩小于相应卤代烷(如 CHX3CHX2Cl)。
四、卤代烷的化学性质
1. 亲核取代反应(通式)
NuX−+R−XR−Nu+XX−
(1)典型反应及反应式
| 反应类型 |
试剂 |
产物 |
反应式示例 |
活性次序/注意事项 |
| 水解 |
NaOH/HX2O |
醇 |
RCl+NaOHROH+NaCl |
卤原子:RI>RBr>RCl>RF;伯卤代烷多走取代,叔卤代烷易消除 |
| Williamson 合成 |
RONa/ROH |
醚 |
ROX− NaX++RX′IRORX′+NaI |
常用伯卤代烷;仲/叔卤代烷易消除 |
| 氰解 |
NaCN |
腈 R−CN |
RBr+CNX−RCN+BrX− |
增长碳链(+1 个 C);NaCN 剧毒 |
| 氨解 |
NHX3(过量) |
伯胺 R−NHX2 |
RCl+2NHX3RNHX2+NHX4Cl |
氨过量避免多取代 |
| 卤原子交换 |
NaI/acetone |
碘代烷 |
RBr+NaIRI+NaBr↓ |
常用于制备碘代烷或定性检验 |
| 与 AgNOX3 |
AgNOX3/EtOH |
硝酸酯 R−ONOX2 |
R−X+AgNOX3RONOX2+AgX↓ |
RI>RBr>RCl;3X∘> 2X∘> 1X∘> CHX3X;用于定性分析 |
2. 消除反应(β-消除,生成烯烃)
(1)脱卤化氢(E1/E2)
- 反应条件:浓碱(KOH、CX2HX5ONa)的醇溶液,加热;
- Saytzeff 规则:优先生成双键取代程度更高的烯烃;
- Hofmann 消除:大体积碱(如 (CHX3)X3COX−)时,优先生成取代程度更低的烯烃。
你原来写的两条“带具体比例的示例反应”属于例题/例数据,若你要求“不要例题”,建议把比例数字删掉,仅保留规则与条件。
(2)脱卤素
3. 与金属反应(生成金属有机化合物)
(1)Grignard 试剂(RMgX)
(2)有机锂(RLi)与二烃基铜锂(RX2CuLi)
- 有机锂制备(示意):
R−X+2LiRLi+LiX
- 二烃基铜锂制备:
2RLi+CuIRX2CuLi+LiI
- Corey–House 合成(偶联):
RX2CuLi+RX′XRRX′+RCu+LiX
五、亲核取代与消除反应机理
1. 亲核取代反应机理(SN1 与 SN2)

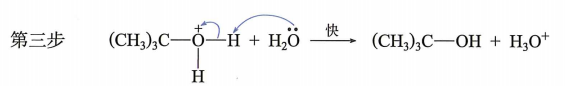
| 机理类型 |
反应步骤 |
速率方程 |
立体化学特征 |
关键特征 |
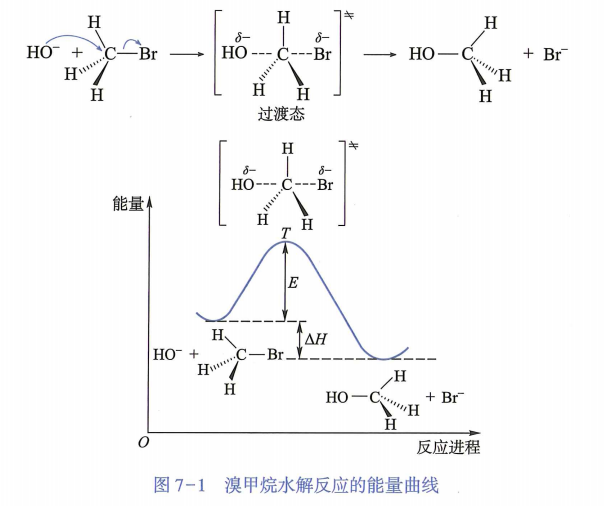
| SN2 |
一步协同:NuX− 背面进攻 α-C,C−Nu 形成与 C−X 断裂同时进行 |
v=k[R−X][NuX−] |
构型翻转(Walden 转化) |
双分子;伯卤代烷为主;一般不重排 |
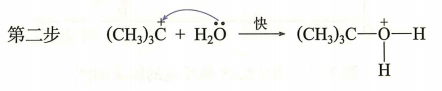
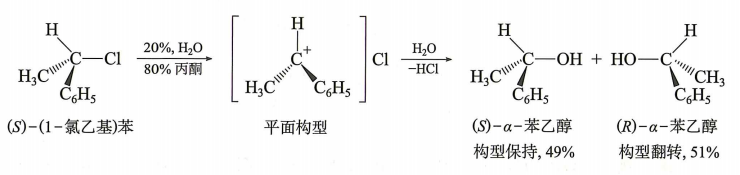
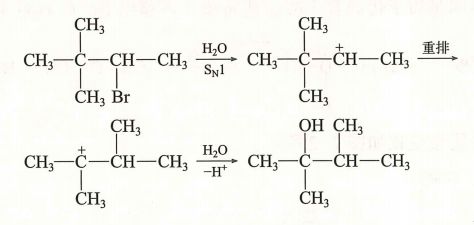
| SN1 |
1)速控步:C−X 异裂生成碳正离子;2)NuX− 进攻 |
v=k[R−X] |
外消旋化(近似) |
单分子;叔卤代烷为主;常伴重排 |
(3)邻基效应(分子内亲核取代)
- 机理:分子内亲核基团进攻形成环状中间体/产物,整体速率可显著加快。
- 特点:常表现为“分子内反应更快”;若经历两次翻转可出现“表观构型保持”。
你原来这段的“反式共平面”写法更适用于 E2 的反式消除条件;若按课本对邻基效应的表述,请以课本原句为准(此处建议你对照 PDF 微调术语)。
2. 消除反应机理(E1 与 E2)

| 机理类型 |
反应步骤 |
速率方程 |
立体化学特征 |
关键特征 |
| E2 |
一步协同:碱夺取 β-H,C−H 与 C−X 同时断裂形成双键 |
v=k[R−X][Base] |
反式消除:β-H 与离去基团需反式共平面 |
双分子;强碱/高浓度;空间与构象限制明显 |
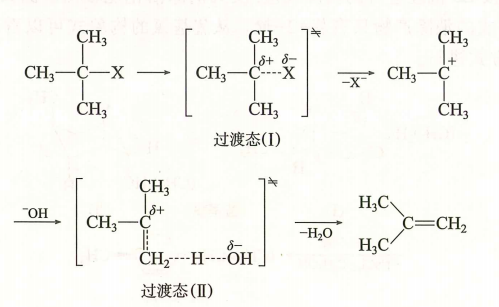
| E1 |
1)速控步:生成碳正离子;2)失去 β-H 成烯烃 |
v=k[R−X] |
一般无严格反式要求 |
单分子;极性溶剂/升温有利;与 SN1 竞争 |
六、影响亲核取代与消除反应的因素
| 影响因素 |
对 SN2 的影响 |
对 SN1 的影响 |
对 E2 的影响 |
对 E1 的影响 |
| 烷基结构 |
CHX3X>1X∘> 2X∘> 3X∘(位阻) |
3X∘> 2X∘> 1X∘> CHX3X(碳正离子稳定) |
一般 3X∘≳2X∘> 1X∘ |
3X∘> 2X∘> 1X∘ |
| 亲核试剂/碱 |
亲核性强、浓度高有利 |
速控步不含亲核试剂 |
强碱、浓度高有利 |
速控步不含碱 |
| 离去基团 |
离去能力强有利:IX−>BrX−>ClX− ≫FX− |
同左 |
同左 |
同左 |
| 溶剂 |
极性非质子溶剂有利(如丙酮、DMF) |
极性质子溶剂有利(如水、酸) |
常随溶剂与碱而变(强碱 + 非质子溶剂常促进) |
极性质子溶剂有利 |
| 温度 |
一般低温更偏取代 |
低温更偏取代 |
升温促进消除 |
升温促进消除 |
(1)亲核性规律
- 同周期:NHX2X−>OHX−>FX−;
- 同族(极性质子溶剂):IX−>BrX−>ClX−>FX−,RSX−>ROX−;
- 同亲核原子:碱性越强一般亲核性越强(溶剂与位阻会改变对应关系)。
(2)卤代烃中 SN2 与消除反应(E2)的竞争规律
在强碱 / 强亲核试剂(如 C2H5ONa/C2H5OH)和较高温度条件下,
卤代烃常发生 SN2 亲核取代反应与 E2 消除反应的竞争。
反应结果主要取决于 α-碳和 β-碳的空间结构。
1. α-碳空间位阻的影响(决定 SN2 是否容易)
-
伯卤代烃:
α-碳空间位阻小,有利于亲核试剂从背面进攻,
SN2 反应容易发生。
-
仲卤代烃:
α-碳具有一定空间位阻,不利于 SN2,
同时具有较多 β-氢,
SN2 与 E2 反应相互竞争。
-
叔卤代烃:
α-碳空间位阻极大,SN2 反应几乎不能发生,
消除反应占主导。
伯卤代烃>仲卤代烃>叔卤代烃(SN2 易→E2 易)
2. β-氢原子数目的影响(决定消除反应程度)
在强碱条件下,E2 反应需要从 β-碳上夺取 β-氢原子:
3. 支链效应的双重作用
支链对反应具有两方面促进消除反应的作用:
-
增大 α-碳的空间位阻,
不利于 SN2 亲核进攻。
-
提高 β-碳的取代程度,
有利于生成更稳定的烯烃(符合扎伊采夫规则)。
4. 总结规律(考试版结论)
-
伯卤代烃:
SN2 为主,消除反应很少。
-
仲卤代烃:
SN2 与 E2 并存,反应比例由结构和反应条件决定。
-
叔卤代烃:
SN2 几乎不发生,E2 为主。
七、卤代烯烃和卤代芳烃的化学性质
1. 活性顺序(核心:C−X 键强度与 p–π 共轭)
烯丙型/苄基型>隔离型>乙烯型/苯基型
- 乙烯型/苯基型:X 连 sp2 碳,p–π 共轭使 C−X 键部分双键化(键能高),难发生常规 SN1/SN2;
- 烯丙型/苄基型:共轭可稳定中间体或降低过渡态能量,使取代/消除更易进行。
2. 乙烯型/苯基型卤代烃的特殊反应
(1)亲核取代反应(需强烈条件或吸电子基活化)
- 加成–消除机理(SNAr):芳环邻/对位连强吸电子基(如 −NOX2、−CN)时,亲核试剂先加成生成负离子中间体,再消除 XX−。
- 消除–加成机理(苯炔机理):无强吸电子基时,强碱条件下先消除形成苯炔,再发生加成。
你原文里含具体反应物/产物与取代定位(如“生成苯胺 + 间甲苯胺”)属于典型例子;如果你坚持“不要例题/实例”,建议把具体反应式删掉,仅保留两种机理的文字描述与条件特征。
(2)消除反应
- 乙烯型卤代烃强烈条件下可脱 HX 生成炔烃(按课本表述掌握条件与机理类型)。
(3)与金属反应
- 乙烯基/芳基卤代烃在一定条件下也可形成相应金属有机物或参与偶联反应(按课本条目掌握)。
3. 烯丙型/苄基型卤代烃的反应
- 亲核取代:可走 SN1 或 SN2,并可能发生烯丙基重排;
- 消除反应:可生成更稳定的烯烃/共轭体系;
- 与金属反应:较易生成 Grignard 试剂,但也可能出现偶联等副反应(以课本总结为准)。
八、氟代烃(特殊类型)
1. 命名
- 系统命名:与其他卤代烃一致,全氟化合物前缀“全氟”,如 CX4FX8(全氟环丁烷);
- 氟利昂(Freon)命名:F−xyz(x=C数-1,y=H数+1,z=F数),如 CClX2FX2(F-12,二氯二氟甲烷)。
2. 制法
- 烃的直接氟化(按课本列举条件与特点);
- 卤原子交换引入 F(如 RCl/RBrRF 的方法体系);
- 重氮盐氟化:ArNX2X+ BFX4X−ΔArF+NX2↑+BFX3。
3. 性质与应用
- 物理性质:沸点低、疏水性强、不溶于水;
- 化学性质:C−F 键能高,多氟/全氟代烃稳定性高,耐酸碱、耐高温;某些一氟代烃在强碱条件下可脱 HF;
- 应用:曾用作冷冻剂(氟利昂)、阻燃剂、材料(如 PTFE)。